Manipulação genética; Eletroporação, CRISPR-Cas9
A eletroporação é uma técnica utilizada em biologia molecular e genética para introduzir material genético em células de forma eficiente. Esse processo envolve a aplicação de pulsos elétricos de curta duração e alta intensidade nas células.
O que é eletroporação?
A eletroporação é um método de transferência de material genético para o interior das células por meio da aplicação de pulsos elétricos. Esses pulsos elétricos criam poros temporários na membrana celular, permitindo a passagem de moléculas como DNA, RNA e proteínas. Esse processo é amplamente utilizado em pesquisas científicas, terapias genéticas e engenharia genética.
Como funciona a eletroporação?
O processo de eletroporação envolve a aplicação de pulsos elétricos de alta voltagem e curta duração nas células-alvo. Esses pulsos elétricos causam uma mudança na permeabilidade da membrana celular, criando poros temporários que permitem a passagem de moléculas grandes. Após a aplicação dos pulsos elétricos, os poros se fecham novamente, garantindo a integridade da célula.
Tipos de eletroporação
Existem dois principais tipos de eletroporação: a eletroporação de baixa voltagem e a eletroporação de alta voltagem. A eletroporação de baixa voltagem é utilizada para transferir moléculas menores, como plasmídeos e oligonucleotídeos, enquanto a eletroporação de alta voltagem é empregada para a transferência de moléculas maiores, como DNA genômico e proteínas.
Aplicações da eletroporação
A eletroporação é amplamente utilizada em diversas áreas da biologia molecular e genética. Ela é empregada em estudos de expressão gênica, terapias genéticas, engenharia genética de plantas e animais, entre outras aplicações. Além disso, a eletroporação também é utilizada em pesquisas científicas para estudar a função de genes específicos e desenvolver novas terapias para doenças genéticas.
Vantagens da eletroporação
Uma das principais vantagens da eletroporação é a sua alta eficiência na transferência de material genético para as células. Além disso, esse método é rápido, simples e não requer o uso de agentes químicos que possam danificar as células. A eletroporação também é altamente versátil, podendo ser aplicada em uma ampla variedade de tipos celulares e moléculas.
Desvantagens da eletroporação
Apesar de suas vantagens, a eletroporação também apresenta algumas desvantagens. Um dos principais desafios desse método é a sua baixa viabilidade em células primárias e tecidos complexos. Além disso, a eletroporação de alta voltagem pode causar danos às células devido ao estresse elétrico, limitando sua aplicação em certos contextos.
O CRISPR/Cas9
O CRISPR/Cas9 (sigla para Conjunto de Repetições Palindrômicas Regularmente Espaçadas em associação com a nuclease Cas9, em inglês) é o nome de uma técnica de biologia molecular capaz de editar (remover, adicionar, trocar) sequências de DNA localizadas em qualquer região do genoma. Essa técnica é baseada em um sistema de memória imunológica presente nas bactérias, usado para protege-las de invasões por vírus (2,3,4).
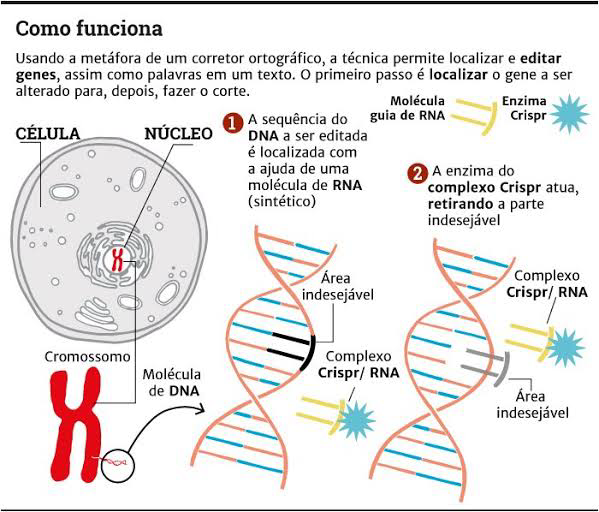
O sistema CRISPR/Cas9 consiste em duas moléculas:
Cas9: uma enzima (nuclease) que atua como um par de “tesouras” que pode cortar as duas fitas do DNA em um local específico no genoma.
RNA guia (gRNA): um pequeno pedaço de sequência de RNA (com cerca de 20 bases de comprimento) localizada dentro de uma estrutura de RNA mais longa. Essa molécula de RNA “guia” a Cas9 para a parte do genoma que deverá ser cortada.
E como o sistema atua?
Conhecendo previamente uma sequência no DNA que se quer alterar (como, por exemplo, uma mutação que causa uma doença), o gRNA é ‘fabricado’ para se ligar (ser complementar) a essa região específica. O gRNA leva a Cas9 até essa sequência complementar, que é então cortada. Logo, o sistema de reparo de DNA, que é natural e intrínseco, ‘conserta’ a região que foi cortada acrescentando a(s) base(s) que foi(ram) removida(s) (2,3,4).
Utilizando o sistema CRISPR/Cas9 é possível induzir o sistema de reparo do DNA. Dessa forma, o sistema é capaz de reparar, silenciar e reprimir genes, entre outras alterações genômicas.
Edição do DNA e o tratamento de doenças
O CRISPR/Cas9 tem um enorme potencial para ser usado como ferramenta no tratamento de diversas doenças que possuem causa genética, como câncer e doenças monogênicas, e doenças infecciosas, como hepatite B e o HIV, por exemplo.
Câncer
O câncer é causado pelo acúmulo de alterações genéticas que levam a multiplicação desordenada das células formando um tumor. Existem vários fatores genéticos já identificados relacionados com a predisposição a desenvolver um tumor, com o local do crescimento do tumor, o seu tamanho e sua malignidade.
Estudos têm o aplicado sistema CRISPR/Cas9 para editar ou remover mutações em genes (oncogenes e proto-oncogenes) que causam essa proliferação celular descontrolada e podem resultar eventualmente em um câncer (5).
Outros estudos têm utilizado o sistema para entender fatores que desencadeiam o crescimento do tumor (tumorigênese) e sua malignidade para selecionar genes alvo para tratamento do câncer a partir de terapia gênica (5).
Além da terapia gênica focada nas alterações que promovem o câncer, resultados promissores foram vistos em estudos clínicos que utilizaram o CRISPR/Cas9 para imunoterapia de pacientes com câncer. Esses estudos retiraram células imunológicas do paciente com câncer (células T ou CAR-T), alteram essas células in vitro utilizando o CRISPR/Cas9 e depois as reintroduziram no organismo do paciente. Os resultados foram positivos, mostrando que as células do sistema imune do paciente conseguiram rejeitar os tumores (6, 7).
Doenças infecciosas
O sistema CRISPR/Cas9 foi originalmente descoberto como um mecanismo de defesa de bactérias contra a invasão de vírus. Logo, é uma ferramenta que naturalmente demonstra ser promissora no tratamento de doenças infecciosas (2).
Vários estudos em células-tronco demonstram o potencial protetor do gene CCR5 contra o vírus HIV: alterações nesse gene conferem resistência à infecção pelo vírus (8, 9).
Em 2018, uma notícia percorreu todas as mídias: um cientista chinês anunciou que duas bebês gêmeas nasceram após os embriões serem geneticamente modificados através da técnica de CRISPR/Cas9. Os embriões tiveram seu DNA editado, mais precisamente o gene CCR5, para que fossem resistentes ao vírus HIV. O cientista relatou que os bebês nasceram saudáveis e sem nenhuma sequela. Porém, a edição genética de embriões é um assunto controverso. O anúncio gerou diversas discussões mundiais e o cientista foi condenado (10).
Além da alteração de genes que conferem resistência ao vírus, o CRISPR/Cas9 se mostrou muito eficaz em um estudo que combinou a técnica de edição de genes com uma terapia anti-retroviral (ART) chamada LASER ART (Terapia Anti-retroviral de Longa Duração e Lenta Efetividade) (11).
A terapia combinada consiste em utilizar o LASER ART, que suprime a replicação do vírus lentamente no organismo e o CRISPR/Cas9 que consegue editar o genoma de células “reservatório” de vírus HIV, que por estarem latentes (“desativados”) não são afetadas pelo LASER ART. No estudo, os cientistas conseguiram eliminar o vírus HIV em ratos infectados (11).
Outras pesquisas exploram a aplicação terapêutica de CRISPR/Cas9 em várias outras doenças, incluindo o vírus influenza, Zika vírus, Dengue, vírus sincicial respiratório (VSR), herpesvírus (HSV) e o poliomavírus neurotrópico humano (JC) (12, 13, 14).
Além disso, várias infecções virais, como o vírus da hepatite B (HBV), o vírus Epstein-Barr (EBV) e o papilomavírus humano (HPV), estão relacionadas ao desenvolvimento alguns tipos de câncer, como câncer de fígado e de colo de útero. Diversos estudos também têm utilizado o CRISPR/Cas9 como estratégia para tratamento desses tipos de câncer, através da inativação do genoma do vírus ou pela inibição da sua replicação (15, 16, 17).
Doenças genéticas
A descoberta do sistema CRISPR/Cas9 revolucionou a engenharia genética e trouxe esperança para o tratamento e cura de muitas doenças. Além das aplicações descritas nos tópicos acima, atualmente, o CRISPR/Cas9 também tem sido utilizado em estudos visando o desenvolvimento de terapia gênica para diversas doenças genéticas.
Diferentes estudos em camundongos demonstraram o potencial do CRISPR/Cas9 para corrigir surdez, Distrofia Muscular de Duchenne (DMD), Hemofilia e Deficiência da alfa1-antitripsina (18, 19, 20, 21).
Um exemplo promissor é a terapia baseada em transplante de células-tronco hematopoiéticas e progenitoras (HSPCs) corrigidas por CRISPR/Cas9 em pacientes com anemia falciforme e a beta talassemia, doenças causadas por mutações no gene da hemoglobina (HBB) (22, 23, 24).
Através do CRISPR/Cas9 os cientistas conseguiram editar o gene HBB das células dos pacientes e recuperar a função normal da hemoglobina. Estudos clínicos estão sendo realizados para comprovar a segurança e eficácia desse tratamento (22, 23, 24).
Limitações
De fato, o CRISPR/Cas9 é a grande esperança da medicina atualmente. Apesar desses (e outros) avanços que o CRISPR/Cas9 trouxe para o mundo e da rápida expansão dos estudos visando o desenvolvimento de novas terapias, muitas pesquisas ainda são necessárias para avaliar a eficiência e, principalmente, a segurança de utilizar essa técnica em humanos.
Estudos também demonstraram que, muitas vezes, o sistema CRISPR/Cas9 erra o alvo e acaba editando outras regiões do genoma. Esse acontecimento é chamado de “off-targets” (fora do alvo) e é um importante fator limitante do uso do CRISPR/Cas9 in vivo em humanos. Ainda é preciso entender como o sistema atua dentro do nosso organismo e quais as consequências de editar nosso genoma, para nós e para as futuras gerações.
Além disso, a edição do DNA levanta muitas questões éticas importantes. Comitês de ética do mundo todo têm discutido a aplicação da edição de genes em embriões.
Comentários
Postar um comentário